基礎研究
白血病および骨髄異形成症候群の転写因子の機能異常による分子病態研究を行っている。主な研究テーマは、RUNX1-MECOMによる白血病の発症機構の解析である。
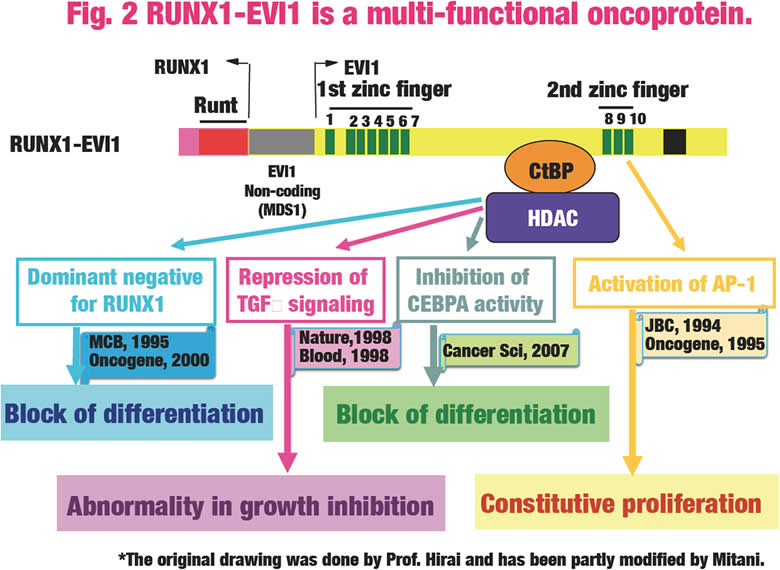
RUNX1-MECOMはt(3;21)の結果形成されるキメラ遺伝子である(Fig.1)。同転座が、慢性骨髄性白血病急性転化例あるいは骨髄異形成症候群白血化例で観察されることから、RUNX1-MECOMは、造血幹細胞腫瘍の病期の進展に関与する遺伝子であると考えられる。また、RUNX1-MECOM はde novo急性巨核芽球性白血病の原因遺伝子でもある。RUNX1-MECOM 分子では、RUNX1のRunt相同領域までのN末領域にMECOMの全長が結合している。このキメラ遺伝子産物には、野生型RUNX1に対するドミナント・ネガティブ効果(分化抑制)、TGFβシグナルの抑制効果(増殖抑制の回避)、CEBPAの抑制効果(分化抑制)、AP1活性の刺激効果(増殖の促進)等の多彩な分子生物学的機能がある(Fig.2)。
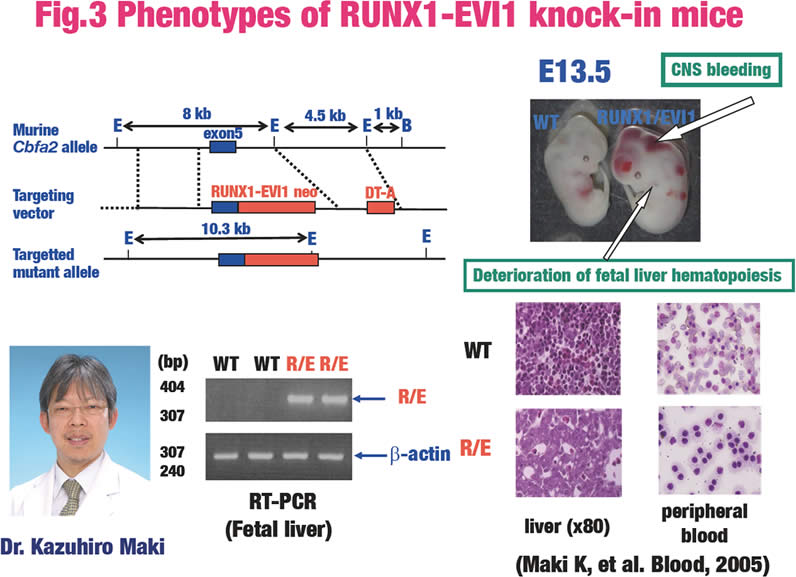
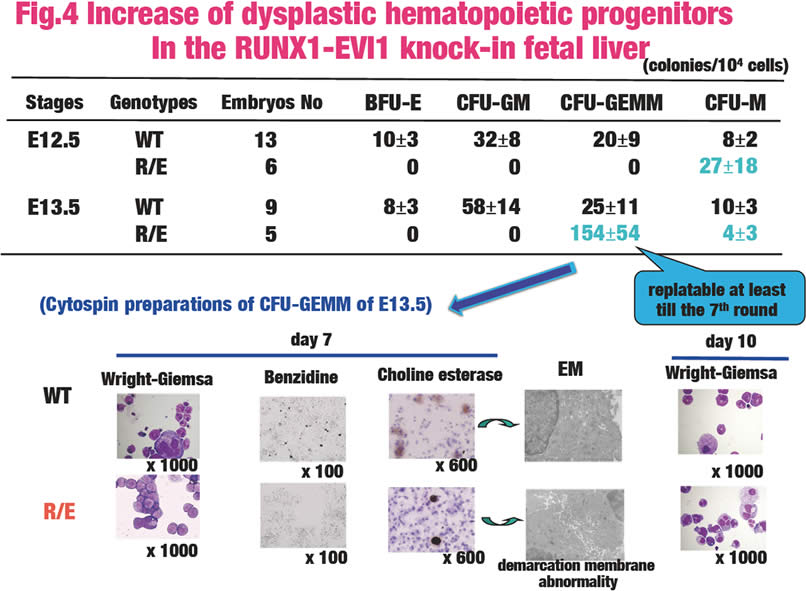
当研究室では、RUNX1-MECOM の機能を発生工学的手法を用いて解析している。RUNX1-MECOMノックインへテロマウスは、野生型RUNX1のノックアウトマウスと同様に、胎生中期に中枢神経系の出血と胎仔肝造血の廃絶により致死となる(Fig.3)。しかしながら、RUNX1-MECOMノックインへテロマウスの胎仔肝には、造血コロニー・アッセイの結果、自己複製能の亢進した造血前駆細胞が存在することが明らかになった(Fig.4)。この造血前駆細胞は、赤芽球への分化能がなく、骨髄球および巨核球の異形成を示した。RUNX1-MECOMノックインキメラマウスは、生後半年で急性巨核芽球性白血病を発症した。このことは、このモデルマウスがヒト白血病を模倣していることを示している。
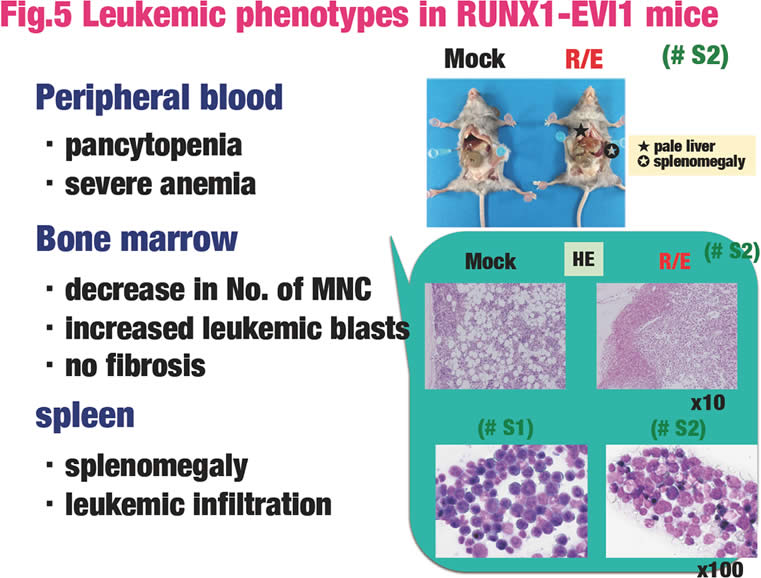
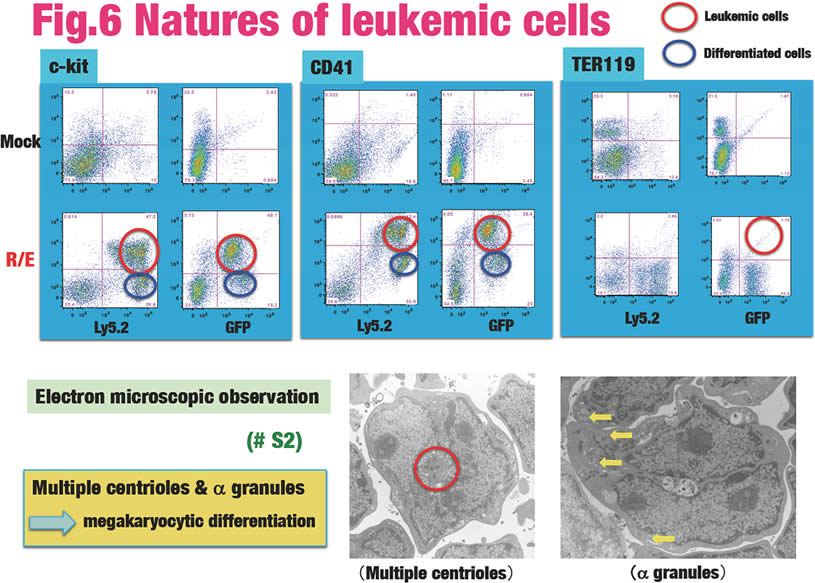
さらに、RUNX1-MECOM型白血病の分子標的療法の開発を目的として、レトロウイルスを感染させた造血前駆細胞を移植することによりモデルマウスを作製している。モデルマウスの一部は、8ヶ月以内に急性巨核芽球性白血病を発症した(Fig.5)。白血病細胞は、c-kit、CD41及びCD31陽性であり、TER119は陰性であった(Fig.6)。白血病細胞は二次移植、三次移植が可能であり、二次移植、三次移植の個体はより早期に白血病を発症する。現在、予後不良のRUNX1-MECOM型白血病の新たな分子標的療法を開発する目的で、白血病骨髄の微小環境の変化を解析している。
最新・血液内科シリーズ FUTURE vol.5

獨協医科大学内科学(血液・腫瘍)教授 三谷絹子
以下より、PDFをダウンロードできます。